Nghiên cứu phương pháp xác định hàm lượng Bạc trong thiếc hàn không chì SAC bằng phương pháp quang phổ hấp thụ nguyên tử ngọn lửa
2.1. Thiết bị và dụng cụ
Các thiết bị sử dụng đều được hiệu chuẩn theo ISO 17025:
3.2 Xây dựng đường chuẩn và đánh giá ảnh hưởng của nền mẫu dựa trên đường chuẩn đo Ag
Xây dựng đường chuẩn trên nền dung môi axit HNO3 1 %, Kết quả thể hiện ở hình 2.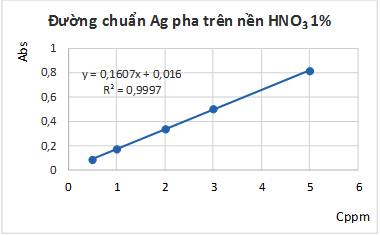
Hình 2. Đường chuẩn Ag pha trên nền axit HNO3 1 %
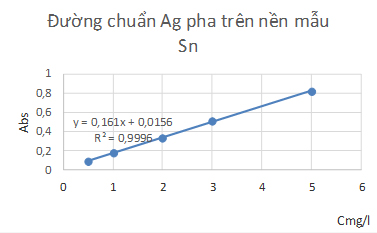
Hình 3. Đường chuẩn Ag pha trên nền dung dịch Sn
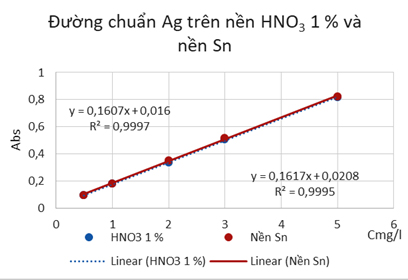
Hình 4. Đường chuẩn của Ag trên nền axit HNO3 1 % và nền mẫu Sn
Bảng 2. So sánh kết quả độ hấp thụ quang của Ag trên hai nền khác nhau
Phan Thị Thanh Hà - Trung tâm Phân tích
1. Mở đầu
Bạc là một trong ba thành phần chính trong hợp kim thiếc hàn không chì SAC, chiếm khoảng 3-4 %. Hiện nay, để xác định hàm lượng Ag trong nền mẫu hợp kim nói chung cũng như hợp kim thiếc hàn không chì nói riêng đã có nhiều phương pháp được ứng dụng như: phương pháp quang phổ hấp thụ nguyên tử, phương pháp quang phổ phát xạ nguyên tử plasma cao tần cảm ứng, phương pháp chuẩn độ…
Theo tiêu chuẩn YS/T 746.2-2010 của Trung Quốc [1], hàm lượng Ag trong thiếc hàn không chì được định lượng bằng hai phương pháp quang phổ hấp thụ nguyên tử AAS và phương pháp chuẩn độ kết tủa với kali thioxianat, chỉ thị Fe2 . Hay trong công bố nghiên cứu của nhóm tác giả người Nhật [2] hoặc ASTM F3139-15 [3] đã đưa ra phương pháp xác định Ag trong thiếc hàn bằng phương pháp quang phổ phát xạ nguyên tử plasma cao tần cảm ứng sau khi mẫu được phân hủy bằng đa axit.
Trong các phương pháp được ứng dụng, thì phương pháp quang phổ hấp thụ nguyên tử ngọn lửa được đánh giá là phương pháp có nhiều ưu điểm nổi trội cũng như thao tác thực hiện đơn giản, ít tốn nguyên liệu hóa chất, có độ nhạy và độ chọn lọc tốt, độ chính xác cao. Đặc biệt phương pháp F-AAS còn phù hợp với điều kiện thực tế tại các phòng thí nghiệm tại Việt Nam.
2. Thực nghiệmBạc là một trong ba thành phần chính trong hợp kim thiếc hàn không chì SAC, chiếm khoảng 3-4 %. Hiện nay, để xác định hàm lượng Ag trong nền mẫu hợp kim nói chung cũng như hợp kim thiếc hàn không chì nói riêng đã có nhiều phương pháp được ứng dụng như: phương pháp quang phổ hấp thụ nguyên tử, phương pháp quang phổ phát xạ nguyên tử plasma cao tần cảm ứng, phương pháp chuẩn độ…
Theo tiêu chuẩn YS/T 746.2-2010 của Trung Quốc [1], hàm lượng Ag trong thiếc hàn không chì được định lượng bằng hai phương pháp quang phổ hấp thụ nguyên tử AAS và phương pháp chuẩn độ kết tủa với kali thioxianat, chỉ thị Fe2 . Hay trong công bố nghiên cứu của nhóm tác giả người Nhật [2] hoặc ASTM F3139-15 [3] đã đưa ra phương pháp xác định Ag trong thiếc hàn bằng phương pháp quang phổ phát xạ nguyên tử plasma cao tần cảm ứng sau khi mẫu được phân hủy bằng đa axit.
Trong các phương pháp được ứng dụng, thì phương pháp quang phổ hấp thụ nguyên tử ngọn lửa được đánh giá là phương pháp có nhiều ưu điểm nổi trội cũng như thao tác thực hiện đơn giản, ít tốn nguyên liệu hóa chất, có độ nhạy và độ chọn lọc tốt, độ chính xác cao. Đặc biệt phương pháp F-AAS còn phù hợp với điều kiện thực tế tại các phòng thí nghiệm tại Việt Nam.
2.1. Thiết bị và dụng cụ
Các thiết bị sử dụng đều được hiệu chuẩn theo ISO 17025:
- Hệ thống quang phổ hấp thụ nguyên tử ngọn lửa (F-AAS)
- Cân phân tích, có độ chính xác đến 0,0001 g.
- Bếp điện, điều chỉnh được nhiệt độ
- Các dụng cụ thông thường tại phòng thí nghiệm.
2.2. Hóa chất
Các loại hóa chất sử dụng đều thuộc loại tinh khiết phân tích:
- Axit nitric HNO3, d=1,51 g/ml;
- Axit sunfuric H2SO4, d= 1,84 g/ml;
- Dung dịch chuẩn gốc Ag, có nồng độ Ag là 1000 mg/l.
2.3. Quy trình xác định hàm lượng Ag trong hợp kim thiếc hàn không chì SAC
Quy trình xác định hàm lượng Ag trong hợp kim thiếc hàn không chì SAC được thể hiện ở hình Hình 1

Hình 1. Quy trình phân tích Ag trong hợp kim thiếc hàn SAC
3. Kết quả và thảo luận
3.1 Tối ưu hóa các điều kiện xác định trên hệ thống F-AAS
Dựa trên các tài liệu tham khảo, khuyến cáo của nhà sản xuất thiết bị và quá trình khảo sát thực nghiệm, các điều kiện xác định Ag trên F-AAS được tối ưu như sau:
Bảng 1. Các điều kiện xác định Ag trên F-AAS
| Nguyên tố | Bước sóng nm |
Khe đo (nm) |
C2H2/Air (ml/phút) |
Cường độ dòng đèn HCL |
| Ag | 328,10 | 0,7 | 2,5/10 | 10 mA |
Khoảng tuyến tính: Sự phụ thuộc của độ hấp thụ quang vào nồng độ Ag có quan hệ tuyến tính trong khoảng từ 0,1 mg/l đến 6,0 mg/l.
Xây dựng đường chuẩnXây dựng đường chuẩn trên nền dung môi axit HNO3 1 %, Kết quả thể hiện ở hình 2.

Hình 2. Đường chuẩn Ag pha trên nền axit HNO3 1 %
Hệ số hồi quy tuyến tính R2 của các đường chuẩn trên đều nằm trong khoảng: 0,995 ≤ R2 ≤ 1. Độ lệch chuẩn các điểm nồng độ được kiểm tra bằng phương pháp tính ngược lại nồng độ của các điểm chuẩn sử dụng để xây dựng đường chuẩn không quá ± 15 %. Đường chuẩn chấp nhận được.
Xây dựng đường chuẩn pha trên nền Sn, Kết quả thể hiện ở hình 3.

Hình 3. Đường chuẩn Ag pha trên nền dung dịch Sn
Hệ số hồi quy tuyến tính R2 của các đường chuẩn trên đều nằm trong khoảng: 0,995 ≤ R2≤ 1. Độ lệch chuẩn các điểm nồng độ được kiểm tra bằng phương pháp tính ngược lại nồng độ của các điểm chuẩn sử dụng để xây dựng đường chuẩn không quá ± 15 %. Đường chuẩn chấp nhận được.
Đánh giá sự ảnh hưởng của nền mẫu Sn đến độ hấp thụ quang của Ag

Hình 4. Đường chuẩn của Ag trên nền axit HNO3 1 % và nền mẫu Sn
Bảng 2. So sánh kết quả độ hấp thụ quang của Ag trên hai nền khác nhau
| Nồng độ Ag (mg/l) | Abs trên nền mẫu Sn | Abs trên nền HNO3 1 % | Độ lệch (abs) |
| 0,5 | 0,0916 | 0,0920 | -0,0004 |
| 1 | 0,1792 | 0,1787 | 0,0005 |
| 2 | 0,3351 | 0,3358 | -0,0007 |
| 3 | 0,5072 | 0,5065 | 0,0007 |
| 5 | 0,8162 | 0,8153 | 0,0009 |
Độ lệch trung bình  = 0,0002
= 0,0002
Độ lệch chuẩn ước đoán cho các độ lệch Sd= 0,0007
Giá trị chuẩn student: ttinh= 0,63
Giá trị chuẩn student tra bảng ở P=0,95 và f= 4: tbảng= 2,132
Giá trị ttính < tbảng (0,63< 2,132) vì vậy có thể kết luận độ hấp thụ ở các mức nồng độ trên hai phép đo khác nhau không có ý nghĩa (nền dung dịch mẫu có chứa hàm lượng Sn tương ứng với nền mẫu không ảnh hưởng đến độ hấp thụ của nguyên tố Ag). Vì vậy nghiên cứu sẽ tiến hành xây dựng đường chuẩn trên nền dung dịch HNO3 1 % để xác định Ag bằng phép đo F-AAS.
3.3 Khảo sát tối ưu điều kiện phân hủy mẫu
Dựa vào tính chất hòa tan của Ag, Ag không đẩy được hydro từ axit ra và không hòa tan được cả trong HCl, hay H2SO4 loãng nhưng Ag dễ dàng hòa tan trong các axit oxit như HNO3 hoặc H2SO4 đặc, nóng:
2Ag 2H2SO4 → Ag2SO4 SO2 2H2O
Ag 2HNO3→ AgNO3 NO2 H2O
Đa số các muối bạc đều khó tan, trong đó có AgCl rất khó tan, chỉ có AgNO3 là dễ tan, Ag2SO4 tan vừa. Các ion Ag sinh ra dễ dàng phản ứng với Cl- trong dung dịch HCl loãng hay cả những clorua tan tạo thành kết tủa trắng vón cục AgCl:
Ag Cl- → AgCl
Vì vậy trong quá trình phân hủy mẫu để phân tích hàm lượng Ag cần tránh các dung dịch có chứa Cl- (ví dụ như HCl). Axit HNO3 đặc là loại dung môi được dùng phổ biến để phân hủy các hợp kim trong xác định hàm lượng Ag. Tuy nhiên đối với các hợp kim chứa Sn, khi phân hủy với HNO3 đặc, nóng sẽ sinh ra Sn(NO3)4, sau đó nitrat này bị thủy phân hoàn toàn tạo axit meta stanic khó tan H2SnO3, điều này ảnh hưởng đến khả năng phân hủy hoàn toàn của mẫu. Theo một số tài liệu tham khảo, để xác định Ag trong hợp kim chứa Sn cần sử dụng hỗn hợp đa axit như: HNO3 và HF; HNO3 và H2SO4. Nghiên cứu tiến hành khảo sát phân hủy bằng hai loại đa axit này.
Kết quả cho thấy khi phân hủy bằng 2 loại dung dịch axit trên đều cho độ thu hồi cao (98-100 %) và độ lặp lại tốt. Tuy nhiên, xét về tính độc hại và chi phí hóa chất thì nghiên cứu lựa chọn hỗn hợp axit HNO3 và H2SO4 để phân hủy mẫu thiếc hàn không chì SAC vì HF là dung môi khá độc và giá thành mua HF đắt hơn nhiều lần so với H2SO4.
3.4. Đánh giá phương pháp
Bài báo đã thực hiện đánh giá phương pháp thông qua độ lặp lại và độ thu hồi. Xử lý thống kê số liệu cho kết quả như sau: Hiệu suất thu hồi (% R) từ 98-99 %, độ lặp lại của phương pháp (% RSD) nhỏ hơn 0,8 %. Độ không đảm bảo đo mở rộng ở mức độ tinh cậy 95 % U của phương pháp là 2,25 %
4. Kết luận
Nghiên cứu đã tối ưu hóa các điều kiện xác định hàm lượng Ag trong hợp kim thiếc hàn không chì SAC bằng phương pháp quang phổ hấp thụ ngọn lửa, phương pháp có độ ổn định và độ chính xác cao. Từ các kết quả nghiên cứu thu được cho thấy phương pháp F-AAS phù hợp cho việc xác định Ag trong hợp kim thiếc hàn không chì SAC, có thể sử dụng quy trình phân tích tại phòng thử nghiệm; đáp ứng nhu cầu đánh giá chất lượng thiếc hàn không chì SAC phục vụ trong công tác sản xuất thiếc hàn tại các doanh nghiệp và yêu cầu xuất nhập khẩu thiếc hàn của các cơ quan quản lý./.
Độ lệch chuẩn ước đoán cho các độ lệch Sd= 0,0007
Giá trị chuẩn student: ttinh= 0,63
Giá trị chuẩn student tra bảng ở P=0,95 và f= 4: tbảng= 2,132
Giá trị ttính < tbảng (0,63< 2,132) vì vậy có thể kết luận độ hấp thụ ở các mức nồng độ trên hai phép đo khác nhau không có ý nghĩa (nền dung dịch mẫu có chứa hàm lượng Sn tương ứng với nền mẫu không ảnh hưởng đến độ hấp thụ của nguyên tố Ag). Vì vậy nghiên cứu sẽ tiến hành xây dựng đường chuẩn trên nền dung dịch HNO3 1 % để xác định Ag bằng phép đo F-AAS.
3.3 Khảo sát tối ưu điều kiện phân hủy mẫu
Dựa vào tính chất hòa tan của Ag, Ag không đẩy được hydro từ axit ra và không hòa tan được cả trong HCl, hay H2SO4 loãng nhưng Ag dễ dàng hòa tan trong các axit oxit như HNO3 hoặc H2SO4 đặc, nóng:
2Ag 2H2SO4 → Ag2SO4 SO2 2H2O
Ag 2HNO3→ AgNO3 NO2 H2O
Đa số các muối bạc đều khó tan, trong đó có AgCl rất khó tan, chỉ có AgNO3 là dễ tan, Ag2SO4 tan vừa. Các ion Ag sinh ra dễ dàng phản ứng với Cl- trong dung dịch HCl loãng hay cả những clorua tan tạo thành kết tủa trắng vón cục AgCl:
Ag Cl- → AgCl
Vì vậy trong quá trình phân hủy mẫu để phân tích hàm lượng Ag cần tránh các dung dịch có chứa Cl- (ví dụ như HCl). Axit HNO3 đặc là loại dung môi được dùng phổ biến để phân hủy các hợp kim trong xác định hàm lượng Ag. Tuy nhiên đối với các hợp kim chứa Sn, khi phân hủy với HNO3 đặc, nóng sẽ sinh ra Sn(NO3)4, sau đó nitrat này bị thủy phân hoàn toàn tạo axit meta stanic khó tan H2SnO3, điều này ảnh hưởng đến khả năng phân hủy hoàn toàn của mẫu. Theo một số tài liệu tham khảo, để xác định Ag trong hợp kim chứa Sn cần sử dụng hỗn hợp đa axit như: HNO3 và HF; HNO3 và H2SO4. Nghiên cứu tiến hành khảo sát phân hủy bằng hai loại đa axit này.
Kết quả cho thấy khi phân hủy bằng 2 loại dung dịch axit trên đều cho độ thu hồi cao (98-100 %) và độ lặp lại tốt. Tuy nhiên, xét về tính độc hại và chi phí hóa chất thì nghiên cứu lựa chọn hỗn hợp axit HNO3 và H2SO4 để phân hủy mẫu thiếc hàn không chì SAC vì HF là dung môi khá độc và giá thành mua HF đắt hơn nhiều lần so với H2SO4.
3.4. Đánh giá phương pháp
Bài báo đã thực hiện đánh giá phương pháp thông qua độ lặp lại và độ thu hồi. Xử lý thống kê số liệu cho kết quả như sau: Hiệu suất thu hồi (% R) từ 98-99 %, độ lặp lại của phương pháp (% RSD) nhỏ hơn 0,8 %. Độ không đảm bảo đo mở rộng ở mức độ tinh cậy 95 % U của phương pháp là 2,25 %
4. Kết luận
Nghiên cứu đã tối ưu hóa các điều kiện xác định hàm lượng Ag trong hợp kim thiếc hàn không chì SAC bằng phương pháp quang phổ hấp thụ ngọn lửa, phương pháp có độ ổn định và độ chính xác cao. Từ các kết quả nghiên cứu thu được cho thấy phương pháp F-AAS phù hợp cho việc xác định Ag trong hợp kim thiếc hàn không chì SAC, có thể sử dụng quy trình phân tích tại phòng thử nghiệm; đáp ứng nhu cầu đánh giá chất lượng thiếc hàn không chì SAC phục vụ trong công tác sản xuất thiếc hàn tại các doanh nghiệp và yêu cầu xuất nhập khẩu thiếc hàn của các cơ quan quản lý./.
Danh mục tin tức
Tin mới nhất
-
 Hợp tác VIMLUKI - Hàn Quốc
Hợp tác VIMLUKI - Hàn Quốc
- Kỷ niệm 45 năm thành lập VIMLUKI
- Toàn cảnh Lễ kỷ niệm 55 năm ngày thành lập Viện Khoa học và Công nghệ Mỏ - Luyện kim
- Hiệp hội Titan Việt Nam
- Phóng sự: 55 năm thành lập VIMLUKI
- Phóng sự: 50 năm thành lập Vimluki
- Highlight lễ kỷ niệm 55 năm thành lập Viện
- Kỷ niệm 40 thành lập Vimluki (p1)
- Kỷ niệm 40 thành lập Vimluki (p2)












